我可以用什么来纯化极性反应混合物?
使用快速色谱法纯化极性反应混合物可能是一个真正的挑战。传统的正相闪蒸需要有毒的二氯甲烷 (DCM) 或氯仿与甲醇进行此类纯化,这可能会产生不可预测且通常不希望的结果。这些相同的化合物通常极性太大,无法保留在反相色谱柱上并在溶剂前沿(在单柱体积或 CV 内)洗脱。如果您遇到其中一个问题,称为 HILIC 的技术可能是解决方案。
那么,您可能会问自己什么是 HILIC? HILIC是亲水相互作用液相色谱法。 这是一种用于分离和纯化极性化合物的技术,这些化合物在反相上不保留和/或对于正相来说极性太大。
一些化学家称这种技术为反相反相色谱,但实际上它是水性正相色谱。与正相一样,HILIC 使用极性固定相柱(硅胶、二醇、胺等)。然而,对于 HILIC,较弱的溶剂通常是乙腈,而强溶剂是水。如您所知,甲醇通常不适用于 HILIC 分离。
直到最近,我执行过的 HILIC 色谱法是在 20 世纪 80 年代我在另一家公司工作时开发的硅胶快速柱 QC 测试(尿嘧啶 + 胞嘧啶在醋酸铵水溶液中)和糖分离。
然而最近,我遇到了一种反应混合物,传统的正相或反相都无法有效纯化,所以我尝试了HILIC。令我高兴的是,这效果很好。
当我尝试纯化烟尿酸与苄胺反应的产物时,就出现了对 HILIC 的需求。虽然我能够通过反相进行一些分离,但我的产品未能很好地从一些副产物中分离出来,这使得我的目标分离具有挑战性,图 1。
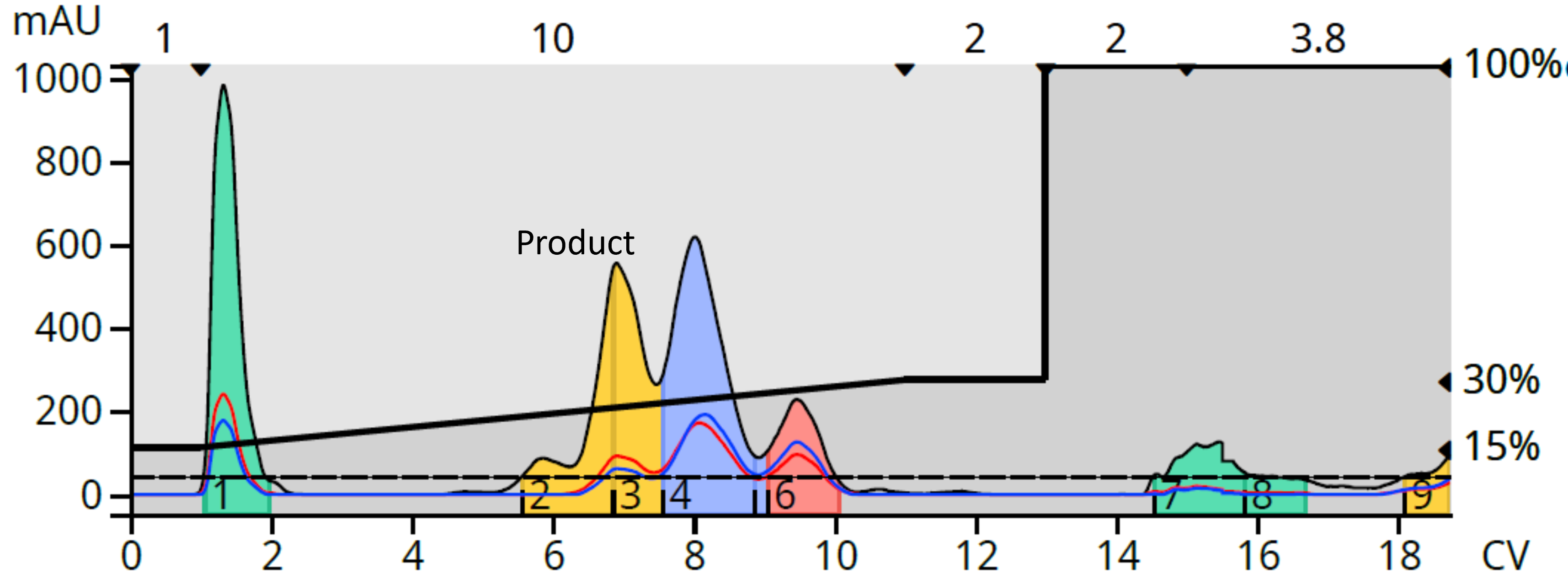
图 1.反相快速色谱分离效果不太理想。
由于反应混合物仅溶于极性溶剂,正相提供的选择有限。我勉强尝试使用硅胶柱使用 DCM-MeOH (0-30%),并实现了良好的分离,尽管放大纯化的空间很小,图 2。
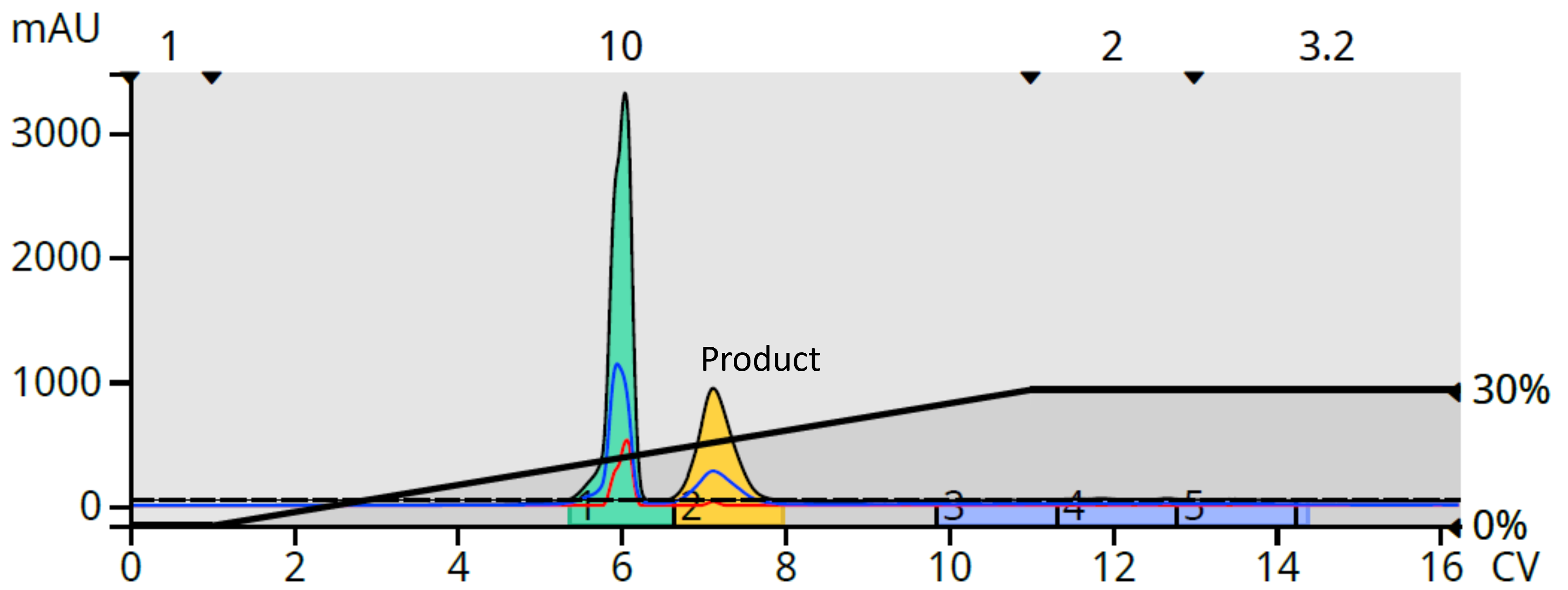
图 2.正相快速色谱分离效果良好,但分辨率有限。
然后,我尝试使用硅胶柱(5 克 Biotage® Sfär HC)和 0-30% 乙腈水梯度进行 HILIC。这种方法提供了满足我需求的最佳结果,解决了我的产品与副产品的问题,图 3。

图 3. HILIC 快速色谱提供了产物和副产物之间的最佳分离效果和出色的分辨率。
HILIC 比传统正相快速色谱法具有优势。正相技术使用危险、有毒的有机溶剂和一次性塑料柱,不是一种环保技术。另一方面,HILIC 确实使用乙腈,但强溶剂是水,产生危险性较小的废物流。 HILIC 还允许硅胶柱在一定程度上重复使用(取决于粗反应混合物的纯度)。在处置之前,我已将硅胶柱重复用于 HILIC 应用 4 到 5 次。
