上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
Amplite 比色法肠激酶活性检测试剂盒价格 5670
产品规格
产品货号
| Ex (nm) | – | Em (nm) | – |
| 分子量 | – | 溶剂 | – |
| 存储条件 | – |
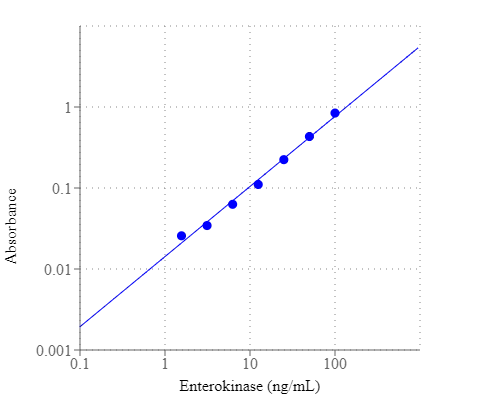
Amplite 比色法肠激酶活性检测试剂盒是美国AAT Bioquest生产的用于酶活性的试剂盒,肠激酶(也称为肠肽酶)是由十二指肠壁中的细胞产生的丝氨酸蛋白酶,并且是人和动物消化系统中的关键酶。 肠激酶将胰蛋白酶原转化为其活性形式的胰蛋白酶,导致随后的胰腺消化酶的活化。 肠激酶的缺乏导致肠道消化障碍。 肠激酶的抑制可能通过抑制参与癌变和转移的蛋白酶而具有抗肿瘤作用。 因此,高度选择性和灵敏的肠激酶检测在生物化学应用中起着关键作用。 Amplite 比色肠激酶活性检测试剂盒为定量肠激酶活性提供了一种灵敏的检测方法。 在肠激酶切割后,肠激酶底物可以通过EK Yellow 在吸光度酶标仪中在405nm处检测。金畔生物是AAT Bioquest的中国代理商,为您提供优质的Amplite 比色法肠激酶活性检测试剂盒。
适用仪器
| 光吸收酶标仪 | |
| 吸收: | 405nm |
| 推荐孔板: | 透明底板 |
样品实验方案
简要概述
1.用稀释的肠激酶标准品(50μL)制备测试样品
2.加入等体积的肠激酶工作液(50μL)
3.在37°C孵育30-60分钟
4.监测OD增加到405nm
溶液制备
1.储备溶液
所有未使用的储备溶液应分成一次性等分试样,并在制备后储存在-20°C。 避免反复冻融循环。
1. EK Yellow 原液(100X):
将50μLDMSO(组分E)加入EK Yellow (组分A)中以制备100X储备溶液。
2.肠激酶底物储备液(100X):
将50μLDMSO(组分E)加入肠激酶底物(组分B)中以制备100X储备溶液。
3.肠激酶标准溶液(10ug / mL):
将50uL ddH2O + 0.1%BSA加入肠激酶标准小瓶(组分D)中以制备10μg/ mL肠激酶原液。
2.标准溶液
肠激酶标准
将10μL10μg/ mL肠激酶标准溶液加入990μL分析缓冲液(组分C)中,得到100ng / mL肠激酶溶液(EK7)。 然后在测定缓冲液中进行1:2连续稀释,以获得连续稀释的肠激酶标准品(EK6-EK1)。 注意:EK标准仅用于阳性对照,不应作为酶活性的定量标准。
3.工作溶液
将50μLEKYellow 储备液和50μL肠激酶底物储备液加入5 mL分析缓冲液(组分C)中; 混合均匀,制成肠激酶(EK)工作溶液(组分A + B + C)。 注意:对于一个96孔板,测定混合物就足够了。 配制的工作溶液不稳定,需快速使用。
样品分析
表1.在96孔透明底微孔板中肠激酶标准品和测试样品的布局。 EK =肠激酶标准品(EK1-EK7,1.56至100ng / mL); BL =空白对照; TS =测试样品。
| BL | BL | TS | TS |
| EK1 | EK1 | … | … |
| EK2 | EK2 | … | … |
| EK3 | EK3 | ||
| EK4 | EK4 | ||
| EK5 | EK5 | ||
| EK6 | EK6 | ||
| EK7 | EK7 |
表2.每个孔的试剂组成
| 孔 | 容积 | 试剂 |
| EK1-EK7 | 50ul | 连续稀释(1.56至100 ng / mL) |
| BL | 50ul | 分析缓冲液(组分C) |
| TS | 50ul | 样品 |
1.根据表1和表2中提供的布局,将肠激酶标准品(EK),空白对照(BL)和测试样品(TS)制备到96孔透明底微孔板中。对于384孔板,使用25μL 每孔试剂代替50μL。
2.在肠激酶标准品,空白对照和测试样品的每个孔中加入50μLEK工作溶液,使总测定体积为100μL/孔。 对于384孔板,在每个孔中加入25μLEK工作溶液,总体积为50μL/孔。
3.将反应混合物在37℃孵育30-60分钟。
4.用吸光度板读数器监测吸光度的增加,在OD为405nm时进行路径检查。
参考文献
Optimization of the fermentation and downstream processes for human enterokinase production in Pichia pastoris
Authors: Melicherova K, Krahulec J, Safranek M, Liskova V, Hopkova D, Szeliova D, Turna J.
Journal: Appl Microbiol Biotechnol. (2016)
A strategy for fusion expression and preparation of functional glucagon-like peptide-1 (GLP-1) analogue by introducing an enterokinase cleavage site
Authors: Liu Y, Ren L, Ge L, Cui Q, Cao X, Hou Y, Bai F, Bai G.
Journal: Biotechnol Lett (2014): 1675
Characterization of a gene family encoding SEA (sea-urchin sperm protein, enterokinase and agrin)-domain proteins with lectin-like and heme-binding properties from Schistosoma japonicum
Authors: Mbanefo EC, Kikuchi M, Huy NT, Shuaibu MN, Cherif MS, Yu C, Wakao M, Suda Y, Hirayama K.
Journal: PLoS Negl Trop Dis (2014): e2644
Do-it-yourself histidine-tagged bovine enterokinase: a handy member of the protein engineer’s toolbox
Authors: Skala W, Goettig P, Brandstetter H.
Journal: J Biotechnol (2013): 421
Fusion expression and purification of four disulfide-rich peptides reveals enterokinase secondary cleavage sites in animal toxins
Authors: Chen Z, Han S, Cao Z, Wu Y, Zhuo R, Li W.
Journal: Peptides (2013): 145
New strategy for specific activation of recombinant microbial pro-transglutaminase by introducing an enterokinase cleavage site
Authors: Wang K, Wang B, Yang HL, Pan L.
Journal: Biotechnol Lett (2013): 383
Immobilization of enterokinase on magnetic supports for the cleavage of fusion proteins
Authors: Santana SD, Pina AS, Roque AC.
Journal: J Biotechnol (2012): 378
Design and efficient production of bovine enterokinase light chain with higher specificity in E. coli
Authors: Chun H, Joo K, Lee J, Shin HC.
Journal: Biotechnol Lett (2011): 1227
The trail of my studies on glycoproteins from enterokinase to tumor markers
Authors: Yamashina I.
Journal: Proc Jpn Acad Ser B Phys Biol Sci (2010): 578
Application of immobilized bovine enterokinase in repetitive fusion protein cleavage for the production of mucin 1
Authors: Kubitzki T, Minor D, Mackfeld U, Oldiges M, Noll T, Lutz S.
Journal: Biotechnol J (2009): 1610
